アンモニアソーダ法(ソルベー法)を解説!目的・覚え方・仕組み・反応順のポイント

アンモニアソーダ法は、自然界にある安価な材料である炭酸カルシウム(CaCO3)から、人類の生活でとても役立つ炭酸ナトリウム(Na2CO3)を5つの化学反応で作り出す方法です。
炭酸ナトリウムは単独で消火剤や入浴剤、洗浄剤(重曹)や石鹸やガラスを含めた生活物資等の製造の原材料に使用されています。
この反応では、途中にアンモニアと二酸化炭素が発生するため、それらを副産物として得ることができ、加えて再反応に使用することも可能です。
アンモニアソーダ法が現在でも使われている理由は、少ない材料でより多くの炭酸ナトリウムを製造することができる点と環境に優しい点が挙げられます。今回は、そんなアンモニアソーダ法の化学反応の原理とその手順の押さえ方を紹介します。
[高校生から始められる]
↓税理士になる方法・勉強方法をチェック!↓
【目次】
①炭酸カルシウムを熱分解して酸化カルシウムと二酸化炭素に分ける反応
②生成した酸化カルシウムを水と反応させて水酸化カルシウムにする反応
③塩化ナトリウム水溶液にアンモニアと二酸化炭素を反応させて炭酸水素ナトリウムと塩化アンモニウムにする反応
④生成した塩化アンモニウムと水酸化カルシウムを反応させて塩化カルシウムとアンモニアと水を生成させる反応
アンモニアソーダ法の概要
アンモニアソーダ法は、1861年にベルギーの化学者ソルベーが考案したことからソルベー法とも呼ばれます。
アンモニアソーダ法のメリットは、発生したアンモニアや二酸化炭素を再び炭酸ナトリウムの製造に使えるため、環境汚染を防ぎ、地球にも優しい製造方法であることです。
化学反応は5段階の反応を用いて行われ、どの段階でどの物質ができるのか、副産物がどの地点で発生するのか。
そのポイントを押さえていくことが理解するために大切です。
①炭酸カルシウムを熱分解して酸化カルシウムと二酸化炭素に分ける反応
アンモニアソーダ法の最初の目的は酸化カルシウムを生み出すことです。
炭酸カルシウムは、カルシウムイオン(二価の陽イオン)と炭酸(二価の陰イオン)が結合しています。
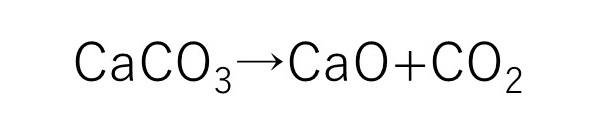
炭酸イオンは二酸化炭素に一個酸素が追加で結合している状態ですが、一番安定するのは二酸化炭素の結合です。
そのため、炭酸は熱を加えることで、より安定して二酸化炭素に結合し、加えてカルシウムイオンと酸素が結合して、酸化カルシウムが生成されます。
炭酸カルシウムは、海の貝殻など自然界に身近にあるものなので、非常に安価で酸化カルシウムを得ることができるのです。
ここで生成した二酸化炭素は③番で再利用されます。
②生成した酸化カルシウムを水と反応させて水酸化カルシウムにする反応
この反応の目的は、強いアルカリ性の塩基を作ることです。
先程生成した酸化カルシウムに、水を入れて反応をさせます。水を入れることで、一価の陰イオンの水酸化物イオン(OH―)を2つ生成し、二価の陽イオンのカルシウムイオンと結合します。その結果、水酸化カルシウムを作り出すことができます。
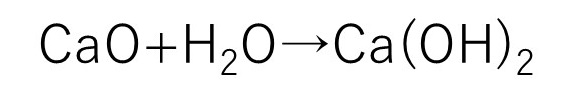
炭酸カルシウムに、水を入れる反応は大きな熱を発生します。
これは、一価の金属イオン(アルカリ金属)であるナトリウムやカリウムと同様、陰イオンがあると容易に結合し、分子構造上安定した構造に成る際に反応熱を発生するからです。
カルシウムイオンも反応性が高く、アルカリ金属と似たような性質を持っており、二価の陽イオンになる性質があることから、アルカリ土類金属に分類されています。
③塩化ナトリウム水溶液にアンモニアと二酸化炭素を反応させて炭酸水素ナトリウムと塩化アンモニウムにする反応
③の反応の目的は塩化アンモニウムを作り出すことです。
この反応で出来た塩化アンモニウムを②で生成した水酸化カルシウムと④で反応させます。
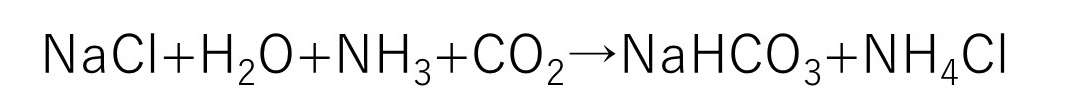
材料は、塩化ナトリウムと水とアンモニアと二酸化炭素になります。ここで重要なのは、塩化ナトリウムがそれぞれ反応し、炭酸水素ナトリウムと塩化アンモニウムになっていることです。
水の中に存在する塩化ナトリウムはそれぞれナトリウムイオン(一価陽イオン)と塩素イオン(一価の陰イオン)となっています。
水に二酸化炭素が存在する場合は、結合して炭酸イオン(一価の陰イオン)となります。加えて、水素イオン(一価の陽イオン)が反応液中に存在している状態です。
その結果、ナトリウムイオン(一価の陽イオン)である水素イオンと炭酸イオン(一価の陰イオン)が結合します。
そしてアンモニウムイオン(一価の陽イオン)と塩素イオン(一価の陰イオン)が結合し、塩化アンモニウムができるのです。
④生成した塩化アンモニウムと水酸化カルシウムを反応させて塩化カルシウムとアンモニアと水を生成させる反応
②のところで生成した水酸化カルシウムと③のところで生成した塩化アンモニウムを反応させます。
この反応の最大の目的は塩化カルシウムを作ることです。
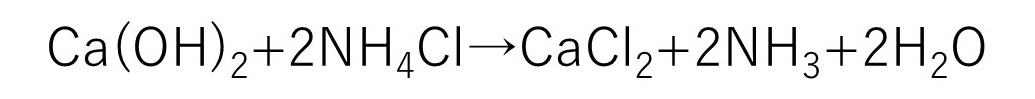
強い塩基である塩化カルシウムは弱塩基の塩化アンモニウムと反応すると、カルシウムイオン(二価の陽イオン)と塩素イオン(一価の塩基)が結合します。
この2つのイオン原子が結合するのは、反応式に存在する原子の中で、電気陰性度が一番離れているためです。
カルシウムが2属(アルカリ土類金属)塩素が17属(ハロゲン属)です。それぞれ強力な陽イオンと陰イオンですから、この2つが生成します。
その後、反応中でアンモニウムイオン(一価の陽イオン)が水素イオンを放出し、アンモニアになります。この水素イオン(一価の陽イオン)と水酸化カルシウムが分解で生成した水酸基(二価の陰イオン)と反応し、2つの水分子とアンモニアが生成されます。
この反応で生成したアンモニアは再利用することができ、③で使うことができます。
⑤炭酸水素ナトリウムに熱分解させ、炭酸ナトリウムと二酸化炭素と水を生成させる反応
③で生成した炭酸水素ナトリウムは熱を与えるだけで分解され、ここで目的の炭酸ナトリウムと水と二酸化炭素が生成されます。
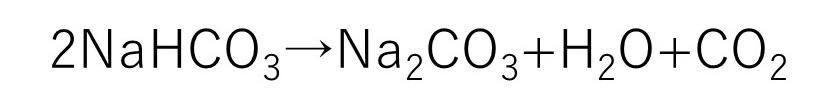
この反応で生成した二酸化炭素は③反応に再利用されます。
①~⑤の反応を合わせた全体の反応式
これが最終的な生成物になります。ここで疑問に思うのは最初にこの塩化ナトリウムと炭酸カルシウムを入れて、炭酸ナトリウムは作れないのかということです。
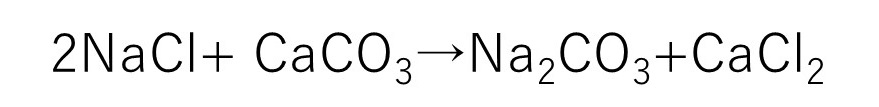
化学式は左辺よりも右辺の生成物が、より安定な分子構造やイオン同士の結合になるというルールがあります。
左辺にある反応する原子や分子が、不安定な構造であり、より安定した結合になるためにお互いが反応し、化合物や分子が生成されます。
この場合、塩化ナトリウムの塩素イオン(17属ハロゲン)、ナトリウムイオン(1族のアルカリ金属)です。そのため、この2つの結合を切り離すエネルギーが右辺の炭酸ナトリウムと塩化カルシウムよりも必要なのです。
わかりやすく身近なもので例えると、塩化ナトリウムはこの反応式の分子の中で一番強力なN極とS極の磁石でくっついている様な状態です。それを無理に剥がすことは容易なことではないため、反応がしやすい別ルート、化学式を経ることで表しています。
そのため、分子の反応のしやすさと最初に使用する原材料の安さを両立させた結果、この様な5つの化学式が必要となったのです。
[高校生から始められる]
↓税理士になる方法・勉強方法をチェック!↓
2.アンモニアソーダ法まとめ
この記事では、アンモニアソーダ法の疑問点である、なぜ5つの反応が必要なのかとそれぞれの化学反応式でできる生成物で特に押さえて欲しい点を中心に、周期表やイオンの生成を踏まえて解説をしました。
化学式を単純に覚えるよりも、「なぜそうなるのか?」を知ると化学の学習も楽しくなります。














