カルボン酸とは?構造やエステルについても解説!

カルボン酸に関する問題は入試などでよく出てきます。
特に構造決定でよく出てくるのですが、こうした問題を解けるようになるためにもカルボン酸について詳しく理解しておきましょう。
ここではカルボン酸とはなんなのかをはじめ、構造やエステルについても紹介します。
問題を解くうえで必要なポイントを抑えていきますので、大事な部分を忘れないよう覚えてください。
[高校生から始められる]
↓税理士になる方法・勉強方法をチェック!↓
【目次】
1.カルボン酸とは何か
カルボン酸というのは、カルボキシ基を持つ化合物のことです。
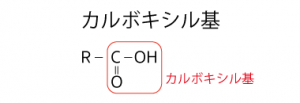
持っているカルボキシ基の数は価数によって表現され、価数が変わると同じ化合物でも別なものとして扱います。
カルボン酸には以下のような化合物があります。
★ギ酸
★酢酸
どれもカルボン酸に該当しますが、価数の違いによっていくつのカルボキシ基を持っているかを判断することになります。
1価なのか2価なのか3価なのかという価数の違いも、必ずチェックしておきましょう。
1分子の中にカルボキシ基が1個ならモノカルボン酸と言い、1分子の中に2個ならジカルボン酸と言い、3個ならトリカルボン酸と名称が変わります。
分子の中に、何個のカルボキシ基があるのかを表現するのが価数とも言えます。
ちなみにカルボン酸について勉強している時や、問題によってはカルボキシ基ではなくカルボキシル基という言葉を目にすることもあるでしょう。
非常によく似た名前でややこしいのですが、カルボキシ基とカルボキシル基は同じものと考えてください。
カルボキシ基と呼ぶ場合もあれば、カルボキシル基と呼ぶ場合もあるだけです。
以前はカルボキシル基と呼ぶことが多かったのですが、現在はカルボキシ基と呼ぶのが主流となっています。
ここでも以下からはカルボキシ基という呼称に統一します。
[高校生から始められる]
↓税理士になる方法・勉強方法をチェック!↓
カルボン酸の特徴・性質について
カルボン酸は炭素数によっても性質が変わります。
炭素数が小さいカルボン酸は水に溶けやすく酸性を示しますが、炭素数が大きくなるに従って水に溶けにくくなる形です。
また炭素数の大きいカルボン酸は、アルコールなどの低極性溶媒に溶けやすくなる傾向が見られます。
さらに分子間で水素結合するので結合力が高く、カルボン酸の異性体であるエステルと比較して沸点が高くなる特徴も持っています。
カルボン酸を沸騰させるためには二量体である水素結合を引き離す必要があり、水素結合を引き離すことで沸騰していきます。このことから沸点が高くなるわけです。
カルボン酸の1つとなるギ酸だけは、アルデヒド基を持つため還元性があります。
2.カルボン酸で見られる反応
カルボン酸には以下の3つの反応が見られます。
★脱水反応
★エステル化
それぞれの反応について、詳しく見ていきましょう。
まず中和反応ですが、カルボン酸は酸性のため塩基と中和反応します。
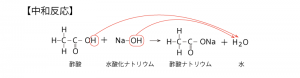
カルボン酸が酸性という性質を利用して、構造決定などでもカルボン酸の検出反応がよく出てきます。
カルボン酸をはじめとした有機物の酸性の強さも重要なので、覚えておきましょう。
もっとも強いのがスルホン酸でその後カルボン酸、炭酸第一電離、フェノール、炭酸第二電離と続きます。
この並びは必ず覚えておください。
脱水反応ですが、これはカルボン酸の2分子間で脱水が発生すると酸無水物が形成されていきます。
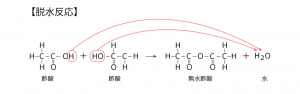
酸無水物が形成される点がポイントなので、忘れないようにしましょう。
最後にエステル化ですが、カルボン酸はアルコールに反応してエステル結合します。
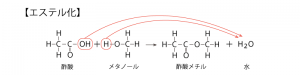
たとえば、酢酸にエタノールを加えることでエステル結合する形です。
酸を触媒にして、エステルを作り出すとイメージすればいいでしょうか。
カルボン酸は酸性ですので、触媒にすることで異性体であるエステルを生み出します。
このようにカルボン酸は、いくつかの反応を見せる化合物となります。
3.カルボン酸の検出反応について
カルボン酸の性質を利用して、構造決定などで検出反応が用いられます。
受験にもよく出る構造決定に関することなので、重要なポイントです。
カルボン酸の検出反応は、炭酸水素ナトリウム水溶液を加えることで行います。
たとえば構成元素がC、H、Oとわかっている状況の時、炭酸水素ナトリウム水溶液を加えてCO2を発生させるのはカルボン酸だけです。
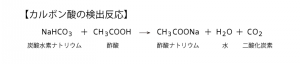
このように検出反応を行うことで、構造決定の役に立つわけです。これがカルボン酸に関する問題で、構造決定がよく出てくる理由です。
特に受験問題では構造決定が出てきやすいので、重点的に学習しておきましょう。
4.カルボン酸の構造
カルボン酸というのは特定の化合物の総称で、同じカルボン酸に該当する化合物でもそれぞれ構造が違います。
構造の違いを理解するとともに、代表的なカルボン酸の構造を覚えておくことも大切です。
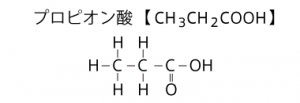
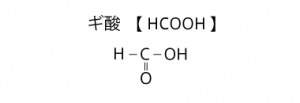
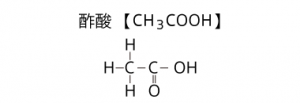
代表的なカルボン酸としてプロピオン酸、ギ酸、酢酸を紹介しましたがこれらも構造は違います。
さらに価数によっても構造が変化します。同じプロピオン酸でも、1価の時と2価の時で構造が変わるわけです。
5.エステルとは?
エステルはカルボン酸の異性体で、分子の中にエステル結合を持つ化合物のことを指します。
カルボン酸の反応の1つであるエステル化でも触れたように、カルボン酸とアルコールに反応することで作られます。
酸を触媒にすることでエステルを作ることが可能なのです。
エステルは中性で水に溶けにくく、有機溶媒には溶けやすいという性質を持っています。
カルボン酸は酸性ですが、異性体であるエステルは中性に変化するので気を付けましょう。
さらにギ酸から作られるギ酸エステルはアルデヒド基を持っていて、還元性を示すのも特徴です。
カルボン酸とアルコールによって作られているので、加水分解すると再度カルボン酸とアルコールが発生します。たとえばエステルを加熱すると加水分解され、カルボン酸とアルコールが生じる形です。元の状態に戻るようなイメージでも良いでしょう。
カルボン酸の異性体ということで、エステルに関しても問題として出題されることがあるので覚えておいてください。
カルボン酸を理解するためにもエステルは重要な存在となります。
6.カルボン酸とホウ素の関係
ホウ素の水素化合物であるボランは、カルボン酸の還元に用いられることがよくあります。
そのためホウ素とカルボン酸の関係は強く、受験問題でもホウ素に関連した問題が出る可能性が考えられます。
正確にはホウ素の水素化合物ボランが重要なわけですが、その関係も抑えておきましょう。
ボランは単独では不安定な物質ですが、ルイス塩基と錯体を作ることで安定性が上昇します。
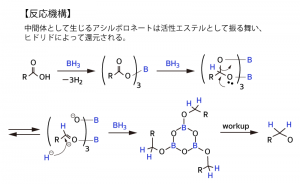
還元力も持つため還元剤として使われ、有機合成の際にカルボニル基や不飽和結合のために使用されます。
特に還元力の強いボランは、カルボン酸の還元にも利用されるのです。
カルボン酸を還元するような問題の中でホウ素、ボランという言葉が出てくることもあるでしょう。
まとめ
カルボン酸は、有機化学のジャンルでは受験によく出る物質の1つです。
構造決定の問題が多いですがその他の問題もありますし、しっかり覚えておきたいところです。
異性体としてエステルがあることも大切で、これも受験によく出る理由となっています。
有機化学を苦手分野としている学生さんも多いと思うのですが、仕組みなどを正しく理解しておけば問題も解けるようになります。
まずはカルボン酸を詳しく知り、関連する問題を確実に解けるようになっておきましょう。
複雑ではありますが順を追って覚えていけば問題ないはずです!














