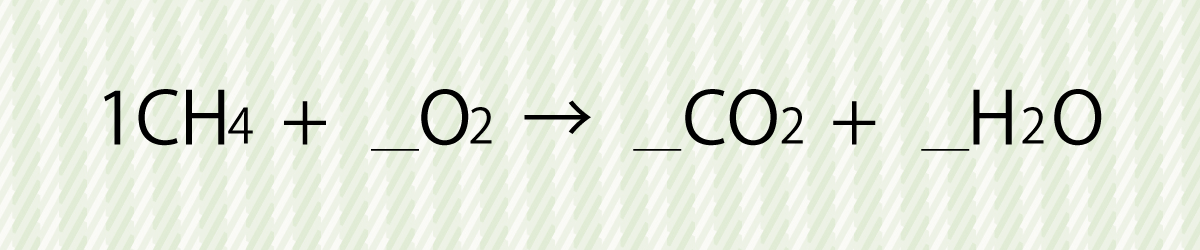化学反応式の作り方を徹底解説!〜基礎から複雑な反応まで〜
化学反応式は化学の基本中の基本です。
理系の方はもちろん、文系の方も化学基礎をセンター試験で使うことでしょう。
高校化学は中学理科と違い、単なる暗記だけでは化学反応式を作ることは難しくなってきます。
そこで今回は、文理問わず化学を使う方を対象に化学反応式の作り方を一から伝授します!
この記事を理解すればどんな反応でも化学反応式を自分で作れるようになるので、しっかりと読み込んで手を動かしてくださいね!
最後には練習問題も載せましたので、解いてみることをオススメします!
[高校生から始められる]
↓税理士になる方法・勉強方法をチェック!↓
【目次】
1.化学反応式って一体何?化学式と何が違うの?
そもそも化学反応式とは何かというところから復習しましょう!
化学反応式は化学反応を化学式を用いて表したものです。
ちょっとわかりづらいですね。
化学では様々な物質が色々な反応を経え違う物質へ変化していく、ということを多く扱います。
これが「化学反応」です。
その「化学反応」ではどんな物質がどれぐらいの割合で反応するのか決まっています。
それを化学式(それぞれの物質がどんな原子から構成されているかを表すもの)を使って表しているのが「化学反応式」なんですね!
例えば
2H2+O2→2H2O(…①)
という化学反応式を皆さん見たことがあるでしょう。
この化学反応式は、どんな化学反応を表しているかわかりますか?
H2という化学式は水素分子を、O2という化学式は酸素分子を、H2Oという化学式は水分子を表しています。
したがって、①の化学反応式は「水素分子二つと酸素分子一つが反応して二つの水分子に変化した」という意味になります。
このように、化学反応式はそれ自体でどんな化学反応が起こったかを表現することができます!
ある意味、化学における「言葉」のようなものですので、これから説明する化学反応式の作り方をマスターしてみてくださいね!
[高校生から始められる]
↓税理士になる方法・勉強方法をチェック!↓
2.目算法を紹介!〜メタンやエタンなどのアルカンに強い〜
それでは、化学反応式の最も基本的な作り方である「目算法」についてこれから説明していきます!
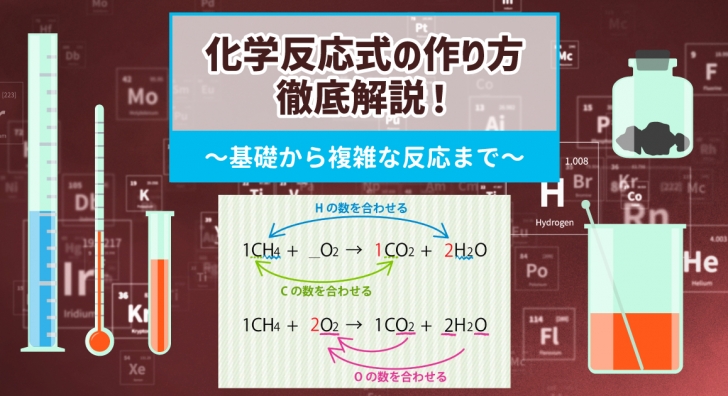
それでは、メタン(CH4)と酸素(O2)が反応(この場合は燃焼反応をします)して二酸化炭素(CO2)と水(H2O)が生成される、という場合を考えてみましょう。
以下、段階ごとに解説していきますね!
⑴まずは、反応物と生成物を確認。
まずはどんな物質が反応してどんな物質が生成されるかを確認します。
この場合は、反応物→メタン、酸素 生成物→二酸化炭素、水
でしたね。
ですので、左辺にCH4・O2を、右辺にCO2、H2Oを配置します。
(化学反応式の真ん中にある矢印を境に、反応物・生成物をそれぞれ配置します。)
これで第一段階は終了です。
(どんな物質が生成するかなどは、問題によっては自分で考えたり、中には暗記する必要のあるものもあるので注意が必要です!)
(2)各化学式に係数をつけ、両辺で元素の種類&数を揃える。
(1)でどんな物質が反応するか確認したら、ここではどんな割合で物質が反応していくかを決定していきます!
この係数の決め方が化学反応式を作る上で大事になってきます。
(1)ではCH4+O2→CO2+H2Oというところまで考えました。
でもこのままだと左辺にはHが4つあるのに右辺にはHは2つしかないし、Oは左辺に2つあるのに右辺には3つあって反応の前後で元素の数が変わってしまいますよね。
中学校で質量保存の法則を習ったかと思いますが、それによると「反応の前後で物質の総重量は変化しない」とのことでした。
だから化学反応式の両辺では元素の種類・数を揃えなければならないんですね。
ここで係数を決めていく際に「目算法」が活躍します!
目算法はその名の通り、激しい計算などはせずに頭の中で係数を考えていく方法です。
実際やっているのを見た方が理解しやすいと思うので、これからやっていきますね!
①まずは、左辺で一番複雑(と思う)物質の係数を1としてみる。
まずは何か一つの物質に着目して、その係数を1としてみましょう。
化学反応式の右辺の物質に注目しても大丈夫ですが、左辺の物質に注目することをお勧めします(ミスが少ない)。
ここでは最も複雑な分子(構成元素の種類が多いなど)に注目するようにしてください!
今回は以下のように、CH4に注目してみましょう。
②質量保存則から、左右で元素の数・種類を合わせていく
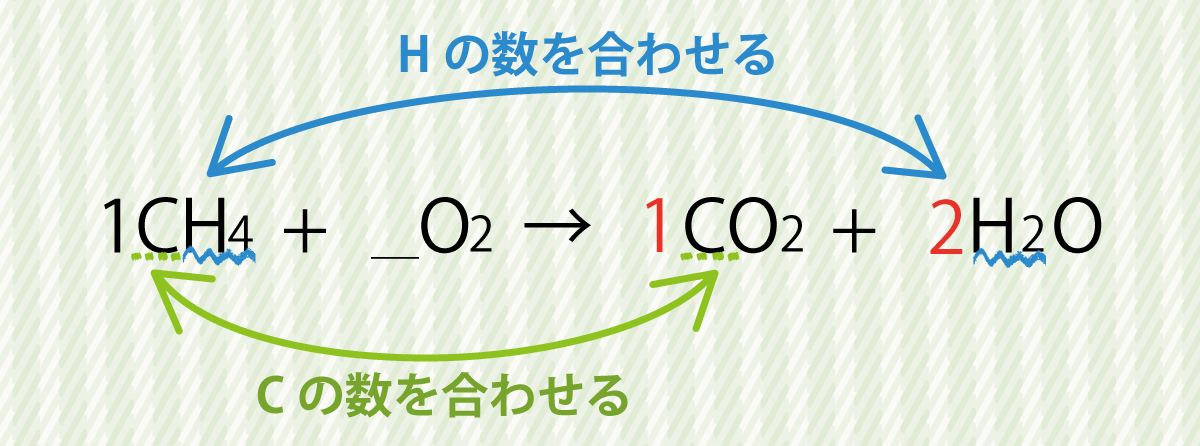
①でCH4の係数を1と置いたので、右辺にもCが1つ、Hが4つあれば良さそうですね。
すると、以下のようにCO2、H2Oの係数が決まってきませんか?
ポイントは、左辺ではCとHはCH4にしか現れないので右辺でCが唯一現れるCO2、Hが唯一見られるH2Oの係数が決まるということです。
③最後に、残った元素の数を合わせていく
ここまででC、Hの数は両辺で合わせられましたが、Oが残ってしまいました。
最後に、この数を合わせていきます。
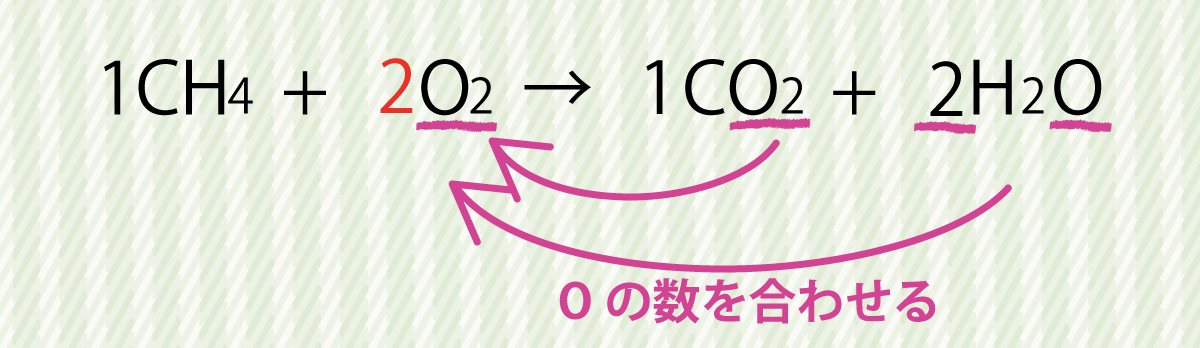
右辺ではCO2が一つ、H2Oが2つあるのでOは合計で4つありますね。
ですので左辺にもOが4つなければなりません。
すると、O2の係数は2となりますね。
このようにして、係数を決めることができました。
④仕上げとして、体裁を整える
①〜③で係数まで決めることができました!
ただ、化学反応式にはいくつかルールがあります。
●係数「1」は省略する
これは、方程式などでy=1x+…と書かないことと同じですね。
●係数は分数ではなく、かつ一番簡単に表す
これは注意が必要です。
この方法だと、例えばO2の係数が7/4になってしまった!ということもありえます。
そういったときは、全ての係数に4をかけて、分数が出現ないようにするなどの対策が必要になります。
また、2CH4+4O2→2CO2+4H2Oというように、全ての係数がある数(今回は”2”)で割り切れるときは必ずその数で割って、最も簡単な数で表すようにしてください。
●左辺と右辺は「→」でつなぐ
数学とは違い、「=」ではなく「→」で両辺を結ぶので、「=」を書かないようにしてください。
以上を踏まえると、今回の化学反応式の例では
CH4+2O2→CO2+2H2Oとなります。
以上が目算法の流れでしたが、目算法はCnH2n+2で表されるアルカンなどの反応では非常に便利な方法です。
また、反応物と生成物をきちんと覚えている場合などにも有効なので、まずは目算法を抑えましょう!
3.未定係数法とは?〜どんな反応にも使える最強の方法〜
これまでは目算法で化学反応式を作ってきましたが、様々な物質が関与する複雑な反応になってくると目算法では厳しくなってくる時もあります。
そこで活躍するのがこれから説明する「未定係数法」です!
この方法は反応物と生成物さえ正しく書けていれば、確実に化学反応式を作り出すことができます。
以下で、先ほどのCH4の例を用いて方法を説明していきます。
(1)よりCH4+O2→CO2+H2Oのように反応物と生成物を書き出すところまでは全く同じですので、これ以降の係数を決定していく流れを説明しますね!
①まず、順に係数をa、b、c、d…と仮に定める。
目算法では複雑な分子の係数を1としましたが、未定係数法では、すべての分子の係数を文字を使って仮置きします。
つまり、aCH4+bO2→cCO2+dH2Oと仮に置きます。
ここまでは簡単ですね!
②質量保存則から、等式をいくつか作って左右で元素の数・種類を合わせていく
言っている意味がよくわからないかもしれませんが、ここで仮置きした文字が活躍します。
実際にやってみますね。
●Cの数が両辺で等しくなるためには、a=cが成立
●Hの数が両辺で等しくなるためには、4a=2dが成立
●Oの数が両辺で等しくなるためには、2b=2c+dが成立
このように、係数を仮置きしているため、例えば左辺にはCはaだけあると考えることができますよね。
ですので両辺で元素の数が同じになるという質量保存則から、以上のような等式がいくつか作れるのです。
この等式ですが、どれか一つの文字を=1と仮定すると解いていくことができます。
今回はa=1(=c)としてみましょう。
すると二つ目の等式よりd=2が、三つ目の等式よりb=2となりました。
したがって1CH4+2O2→1CO2+2H2Oとなりましたね。
③仕上げとして、体裁を整える
②までできたら化学反応式は作れたも同然です。
「目算法」と同じように、係数をルールに従って整えていきましょう!
「未定係数法」でも置いた文字が分数になる場合はあるので、先ほどのルールを思い出しながら化学反応式を完成させましょうね。
今回は、1は書かないというルールからCH4+2O2→CO2+2H2Oとなります。
以上、化学反応式を作る二つの方法を紹介してきましたが、いかがでしたか?
目算法は慣れれば素早く化学反応式を作れ、未定係数法は時間はかかるものの確実に化学反応式を作れるというメリットがそれぞれあります。
どの化学反応でどちらの方法を使えばいいかは問題演習していくことで少しづつ分かってくるので、コツコツと問題を解いていってください!
4.化学反応式を作ってみよう!〜重要例題2選〜
先ほど問題演習が大切と書きましたが、実際にいくつか問題を解いていきましょう!
例題を載せますので、まずは今までの解き方をなぞる形で解いてみてください!
問題1.ブタン(C4H10)が完全燃焼した時の化学反応式を書け
解答:この問題ではブタンのみしか化学式が与えられていませんね。
しかし、いくつかヒントが隠されています。
・「燃焼」という反応の際には酸素(O2)が必要となるので、反応物にはO2が含まれる
・アルカン(CnH2n+2)の「完全」燃焼という反応なので、生成物は二酸化炭素(CO2)と水(H2O)である(※要暗記)
これらから、反応物と生成物が何かというということがわかりました。
それでは目算法で化学反応式を作っていきましょう。
まずはC4H10+O2→CO2+H2Oとかけますね。
それでは最も複雑な分子であるC4H10の係数を1としてみましょう。
すると右辺でCが4つ、Hが10個存在しなければならないのでCO2の係数は4、H2Oの係数は5となります。
これより、右辺ではOが4×2+5×1=13個あるとわかりましたので、これに合わせると左辺のO2の係数は13/2となりますね。
以上から1C4H10+13/2O2→4CO2+5H2Oという化学反応式ができましたが、まだ不十分です。
”係数に分数はダメ”というルールを思い出すと、全体の係数を2倍して2C4H10+13O2→8CO2+10H2Oとなります。…答え
問題2.アンモニア(NH3)と酸素(O2)が反応し、一酸化窒素(NO)と水(H2O)が生成した。この化学反応式を書け。
解答:今回は反応物と生成物が与えられていますね。
もちろん、目算法で解答してもいいですが、ここでは未定係数法で解いてみますね。
まずはaNH3+bO2→cNO+dH2Oと、反応物と生成物を書き出し、それぞれの係数を文字で置きます。
●Nに注目してa=c
●Hに注目して3a=2d
●Oに注目して2b=c+d
以上のように式が建てられましたね。a=1として解いてみると、a=c=1、d=3/2、b=5/4となりました。
したがって1NH3+5/4O2→1NO+3/2H2Oとなりますね。
”係数に分数はダメ”というルールを思い出すと、全体の係数4倍して4NH3+5O2→4NO+6H2Oとなります。…答え
まとめ
この記事では、二つの問題を解いていきましたが、いかがでしたでしょうか?
初めはなんとなく化学反応式を作る方が楽かもしれません。
ですが複雑な反応でも化学反応式を書けるようにするためには、「目算法」や「未定係数法」を身につける必要があるので、しっかりとこのページを復習して理解してくださいね!
やり方を身につけるためには、繰り返しますが問題演習が不可欠なのでお持ちの問題集などで繰り返し練習して下さい!!
ちなみにイオン化反応式というものがいずれ出てくるかとは思いますが、その際はイオン化傾向などの知識を踏まえつつ化学反応式を考えていくこととなりますので、まずは普通の化学反応式を作れるようにしましょう!
化学反応式を確実にマスターして、応用問題などにチャレンジしていけるようにしましょうね!