比熱とは?例題を用いて比熱を含めた熱力学をマスターしよう

熱に関する問題は、物理だけでなく化学でも出題されます。
化学で出題される熱の問題は、反応熱に関する問題や気体の圧力や体積と関連する問題です。
一方で、物理で出題される熱の問題は、分子運動に基づいた熱力学の問題です。
これには、気体の状態方程式なども含まれます。
この記事では、高校物理の熱力学の基礎についてまとめ、特に比熱について解説してゆきます。
【PR】勉強を効率的に継続して、志望校に合格したい方必見!

↓無料ダウンロードはこちら↓
1. 比熱を学ぶ前に!熱力学の基本である熱と熱容量について
高校物理で点数を取るためには、用語を正確に理解することが大切です。
正確な用語の理解と、定義をしっかりおさえていることが、物理の点数を取るための最低条件です。
例えば日常生活では、熱という言葉と温度という言葉を同様に扱うことがありますが、物理では明確に区別しておく必要があります。
物理で熱といえば、通常「熱量」のことを指します。
熱量の単位はJ(ジュール)です。
熱量と温度の理解が、熱力学の基本中の基本です。
物質がもつ熱量は(物体の状態によらず)その物質を構成する分子の運動によって生まれています。
分子や固体中の原子は、常に基準となる位置を中心に振動運動をしていて、振動の振幅が大きくなるほど、その分子や原子のもつエネルギーは大きくなります。
突き詰めれば、このエネルギーの集合体(語弊のある表現ですが)こそが、その物体が持っている熱量です。
では「熱量」と「温度」の違いは何でしょうか。
「熱量」とは、原子や分子がもつエネルギーの合計熱の合計量のことです。
一方、「温度」は原子や分子1個当たりが持っている平均のエネルギーのことです。
例えば、沸騰した水について考えましょう。
通常、水は100℃で沸騰します。
沸騰した水は量にかかわらず、その「温度」は100℃です。
一方、「熱量」を考えると、水の量が増えるほど「熱量」は増えます。
これは「熱量」が「エネルギーの合計」であり、「温度」が「平均のエネルギー」を指しているからです。
余談ですが、分子の振動が最も小さくなったときに、その物体がもつ熱量が最も小さくなり、それ以下の温度になることがありません。
その温度が、よく耳にする「絶対零度」です。
厳密には絶対零度でも原子の振動が完全に止まっているわけではないのですが、高校で学習する範囲ではないので、割愛します。
詳しくは、大学で量子力学の不確定性原理を勉強してください。
次は、「熱容量」についてです。
「熱容量」とは、ある物体の温度を1℃(=1[ K ] )上げるのに必要な熱量のことです。
例えば、ある物体に500 [ J ] の熱量を与えたときに、温度が5 [ K ] 上がったとき、1 [ K ] 温度を上げるのに100 [ J ] の熱量が必要だったことになります。
この100 が、この物体の熱容量です。
熱容量の単位は [ J / K ] です。
公式化すると、熱容量 C [ J / K ] の物体に熱量Q [ J ] を与え、その物体の温度が T [ K ] 上昇したとき、
Q = CT
となります。
熱容量については以下の記事にまとめてありますので、合わせてご確認ください。
↑熱容量とは?熱量保存の法則や比熱との関係、求め方・計算問題までを即理解!
2. 比熱とは?公式解説付き
比熱は、物質の熱的な性質を示す量です。
その物質1 [ g ](あるいは1 [ kg ] など)の温度を 1 [ K ] 上げるのに必要な熱量を「比熱」と言います。
比熱の単位は [ J / g ・K ] や [ J / kg・K ] などです。
この段階で「熱容量」と「比熱」の違いがわかりましたか。
「熱容量」も「比熱」も、言い換えれば「ものの温まりやすさ」に関する性質を表すものです。
共にどれだけ熱(熱量)を与えれば、温度が上がるかを表しています。
熱容量が表すのは、その物体全体を1 [ K ] 温めるのに必要な熱量です。
同じ物質(例えば鉄)であっても、100 [ g ] に対する熱容量と、200 [ g ] に対する熱容量は異なります。
一方で比熱が表すのは、その物質(例えば鉄)1 [ g ] を温めるのに必要な熱量ですので、その物質の熱的な性質そのものです。
比熱c [ J / g・K ] の物質が m [ g ] あり、温度をT [ K ] 上げるのにQ [ J ] の熱量が必要だったとすると、
Q = mcT
と表すことができます。
これが、比熱の公式です。
言い換えると、物質が持っている熱量 Q [ J ] は、物質の量 m [ g ] と温度 T [ K ] に比例し、その比例定数cが比熱である、と言えるでしょう。
例題1
0 ℃の氷300 [ g ] を熱して全て100℃の水蒸気にしたい。熱を無駄なく使えるとするなら、どれだけの熱量が必要か。ただし、氷の融解熱を340 [ J / g ]、水の蒸発熱を 2300 [ J / g ] とし、水の比熱を4.2 [ J / g・K ] とする。
解答・解説
物質に熱を与える、ということは、その物質の分子の運動エネルギーを増加させる、ということです。
突き詰めれば、分子の運動エネルギーの集合体が、私たちが観測している「熱量」であることは、既に説明しました。
氷(固体)に熱を加えれば水(液体)になり、さらに熱を加えることで温度を上げ、100℃に達した後、水蒸気(気体)になります。
物質の状態が変化しなければ、加えた熱は運動エネルギーに変換される、つまり温度を上げるために使われますが、氷から水、水から水蒸気になるときには、固体結晶を壊したり、分子同士の結びつきを緩くするために熱が使われます。
このときに使われる熱を、融解熱や蒸発熱と言います。
この問題では、
<氷>→(融解熱)→<0℃の水>→(比熱)→<100℃の水>→蒸発熱→<水蒸気>
といったように、それぞれの状態に応じた熱量の計算をしなくてはなりません。
氷を融解させて水にするためには、「氷の融解熱を340 [ J / g ] 」となっていますから、1 [ g ] あたり、340 [ J ] 必要ということになります。
よって、
340 ✖️ 300 = 102000[ J ]
です。
同様に蒸発熱も計算しましょう。
最後に水を100℃に温めるのに必要な熱量を、比熱を用いて計算します。
これらを全て合計すると、
「 918000[ J ] 」
というように答えを導くことができます。
例題2
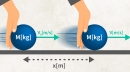
質量 m1で比熱が c2、温度がt1 の液体がある。この液体に反応しないような、質量m2 で比熱がc2 、温度が t2の金属を液体に入れ、充分にかき混ぜた。充分時間が経過した後の温度を求めよ。ただし、液体の容器の熱容量は無視するものとする。
解答・解説
液体に金属などの固体を入れるような問題は頻出です。
ポイントは「外部との熱の出入りがあるか、ないか」です。
外部との熱の出入りがない場合は、全体のエネルギーが保存されるため、それを使って問題を解きます。
熱の出入りがある場合には、それも含めて立式する必要があります。
この問題では、容器の熱容量を無視しますから、エネルギー保存を使いましょう。
充分に時間が経過すると、金属と液体の温度は同じになります。
液体に金属を入れる前に持っていた液体と金属の熱量の合計は、充分時間が経過したあとの水と金属の熱量の合計と一致しますから、求める温度をtとおくと

3. おわりに
最後までご覧くださってありがとうございました。
この記事では、熱力学の基本と比熱、熱容量などについてまとめました。
「比熱」というのは、ものの温まりやすさを表す指標で、「比べるのなら質量を合わせて比べた方がいい」という発想で生まれたものです。
それにたいして、「物質量(モル)」を揃えて比べよう、という発想で生まれた「モル比熱」というものもあります。
熱力学の基本がわかったら、このあとの「気体の状態方程式」や「分子運動と内部エネルギー」「熱力学第一法則」などの理解も進みます。
まずは、基本をしっかりと理解することから始めましょう。
ご参考になれば幸いです。